¿QUÉ ES EL NIRSEVIMAB?
Es un anticuerpo monoclonal (medicamento), inyectable de acción prolongada, efectivo y seguro contra el Virus Respiratorio Sincicial (VRS).
¿QUÉ LABORATORIO LO PRODUCE?
El laboratorio SANOFI, con el nombre comercial de Beyfortus
¿CUÁLES SON LOS GRUPOS QUE RECIBIRÁN ESTE MEDICAMENTO, POR PARTE DEL MINISTERIO DE SALUD?
Recibirán el medicamento cuatro grupos objetivos
Se mantiene la vacunación a recién nacidos a partir del 1° de marzo de 2025.
Serán inmunizados solo en maternidades y unidades de Neonatología de establecimientos públicos y privados en convenio.
Lactantes nacidos a partir del 1 de octubre 2024.
Lactantes de riesgo:
a) Lactantes en segunda temporada nacidos a partir del 1° de abril 2023:
Prematuros < 32 semanas o < 1.500 gr de peso al nacer.
Lactantes con cardiopatías congénitas hemodinámicamente significativas no resueltas o cardiopatía cianótica secundaria a cardiopatía de alta complejidad.
b) Lactantes en segunda temporada nacidos a partir del 01 de abril 2024:
Prematuros de 32 a 34+6 semanas y con peso al nacer entre 1.500 a 2.500 gr.
c) Recién Nacidos o lactantes sometidos a circulación extracorpórea (nacidos a contar del 30 de septiembre del 2023):
Administrar 1 dosis adicional.
Otros lactantes de riesgo definidos por la autoridad.
¿POR QUÉ ES IMPORTANTE QUE RECIBAN ESTA INMUNIIZACIÓN CONTRA EL VRS?
Porque el Virus Respiratorio Sincicial (VRS) es reconocido como una de las causas más frecuentes de enfermedades infantiles y es la causa más común de hospitalización en los lactantes. Es una enfermedad grave, que puede ser mortal.
¿QUÉ SE ESPERA LOGRAR CON ESTA ESTRATEGIA?
Se espera prevenir la enfermedad grave y la mortalidad por el Virus Respiratorio Sincicial (VRS) en población objetivo que vive en Chile, previo a la temporada de alta circulación del virus.
¿ES UN MEDICAMENTO SEGURO Y EFICAZ?
Demostró una alta eficacia y seguridad en los ensayos clínicos y en la utilización durante el año 2024, cuando se realizó la aplicación del anticuerpo, con un excelente cumplimiento superando la meta del 80% . A lo anterior se suma que no se presentaron defunciones asociadas a VRS en el grupo objetivo de la campaña.
Adicionalmente, cuenta con la aprobación y recomendación de uso por parte de las principales agencias del mundo.
El Instituto de Salud Pública autorizó el registro sanitario de nirsevimab el 28 de diciembre de 2023. En tanto, el Comité Asesor en Vacunas y Estrategias de Inmunización (CAVEI) El CAVEI entregó su recomendación el 28 septiembre 2023.
El Ministerio de Salud recibió el pronunciamiento del Comité de Neonatología de la Subsecretaría de Redes Asistenciales, quienes emitieron una recomendación positiva en relación con la incorporación de nirsevimab, con acceso universal, y de reemplazar la administración de palivizumab por nirsevimab.
¿CUÁL ES LA DOSIS Y LA VÍA DE ADMINISTRACIÓN?
La dosis la determina el personal de salud de acuerdo a los antecedentes del lactante y recomendaciones del fabricante, no obstante, este último señala:
Dosis
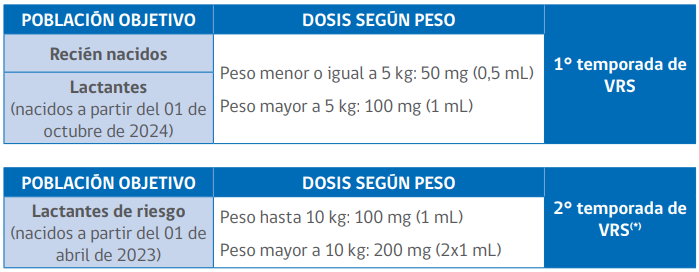
Vía de administración
Intramuscular.
¿CUÁLES SON LAS REACCIONES ESPERABLES TRAS LA APLICACIÓN?
Al igual que con otros medicamentos inyectables, las reacciones pueden ser, dolor, inflamación o hinchazón en el lugar de vacunación. También puede presentar fiebre y erupción en el sitio de punción.
Frente a estas reacciones:
Dar a tomar bastante líquido.
Colocar compresas frías el lugar donde se aplicó (temperatura ambiente) si existe dolor local.
No abrigar en exceso.
No tocar la zona donde se ha vacunado.
Controlar la temperatura en caso de ser necesario.
Usar medicamentos para dolor y/o fiebre recomendados por el profesional de salud.
Si presenta un síntoma persistente o tiene dudas, puede solicitar orientación llamando a Salud Responde al 600 360 7777 opción 1.
CUÁNTO DURARÁ ESTA CAMPAÑA?
Se prolongará durante la temporada de circulación de Virus Respiratorio Sincicial (aprox. hasta el 30 de septiembre 2025).














